Особенности органических реакций
- В реакциях органических соединений, как правило, изменения затрагивают только часть молекулы и ее основная конструкция (углеродный скелет) сохраняется. Например:
C6H5-CH2-Cl + H2O В случае неорганических реакций более характерен распад соединения на ионы или атомы, из которых образуются совершенно новые конструкции: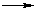 C6H5-CH2-OH + HCl
C6H5-CH2-OH + HCl
Al2S3 + 6H2O = 2Al(OH)3↓ + 3H2S↑
- Большинство органических реакций протекают значительно медленнее реакций неорганических веществ и обычно не завершаются полностью вследствие их обратимости.
Обратимая реакция - химическая реакция, которая при одних и тех же условиях может идти в прямом и в обратном направлениях.
Необратимой называется реакция, которая идет практически до конца в одном направлении. - Многие органические реакции являются сложными и включают несколько элементарных стадий.Элементарная стадия (элементарная реакция) – единичный акт образования или разрыва химической связи при непосредственном взаимодействии частиц (молекул, ионов, радикалов).
Пример 3-х стадийной реакцииПревращение этанола в этилен
1-я стадия - протонирование спирта (в присутствии кислоты),
2-я стадия - отщепление воды с образованием этил-катиона,
3-я стадия - стщепление протона и образование двойной связи.
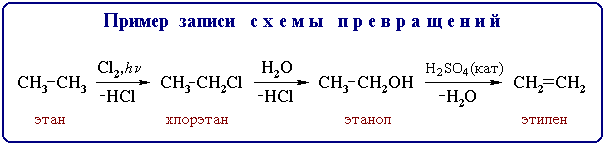
Примечание: последовательность нескольких реакций принято изображать в виде схемы (цепи) превращений, в которой действующий на органическое соединение реагент записывается над стрелкой, а выделяющийся побочный продукт – под стрелкой со знаком "минус":