Пространственные (стерические) эффекты
Реакционная способность соединений зависит не только от электронных эффектов заместителей, но и от их пространственного строения – размеров и относительного положения в молекуле. Такое влияние, называемое пространственным или стерическим эффектом, как правило, тем больше, чем ближе расположен объемный заместитель к реакционному центру молекулы.
Объемные группы могут пространственно блокировать реакционный центр и снижать реакционную способность молекулы. Так, скорость реакции присоединения по связи С=О убывает в ряду:
формальдегид > ацетальдегид > ацетон > ди-трет-бутилкетон

Видеоопыт
Взаимодействие фенола с гидроксидом натрия
| Источник: Постановка опыта и текст – к.п.н. Павел Беспалов. |
Фенол по сравнению с одноатомными спиртами проявляет более сильные кислотные свойства. Он способен реагировать с растворами щелочей. К водной эмульсии фенола прильем несколько капель раствора гидроксида натрия. Образуется прозрачный раствор фенолята натрия.
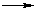 C6H5ONa + H2О
C6H5ONa + H2ОСильные кислоты вытесняют фенол из фенолята:
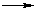 C6H5ОН + NaHSО4
C6H5ОН + NaHSО4
Оборудование: пробирки, штатив для пробирок, шпатель.
Техника безопасности. Соблюдать правила работы с ядовитыми веществами. Фенол вызывает ожог кожи. Не допускать попадания фенола на кожу. Соблюдать правила работы со щелочами и их растворами.
Однако, фенолы с объемными заместителями, экранирующими группу ОН, в эту реакцию не вступают:









