Радикальные реакции
Реакции, в которых происходит гомолитический разрыв связей и образуются свободно-радикальные Свободный радикал – частица с неспаренным электроном: •Cl, •R и т.п. промежуточные частицы, называются радикальными реакциями.
Новые связи в радикальных реакциях образуются по обменному механизмуПри обменном механизме в образовании ковалентной связи участвуют одноэлектронные атомные орбитали связываемых атомов, т.е. каждый из атомов предоставляет в общее пользование по одному электрону.
.
Пример – реакция радикального замещения при хлорировании метана.Общая схема реакции:
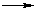 CH3Cl + HCl
CH3Cl + HCl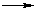 2 Cl• (на свету)
2 Cl• (на свету)
Cl• + H–CH3
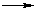 HCl + •CH3
HCl + •CH3
•CH3 + Cl2
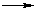 CH3Cl + Cl• и так далее.
CH3Cl + Cl• и так далее.Анимация
Механизм радикального замещения обозначается символом SR
(по первым буквам английских терминов: S – Substitution [замещение], R – Radical [радикал]).
(по первым буквам английских терминов: S – Substitution [замещение], R – Radical [радикал]).
Реакции с участием свободных радикалов характерны для соединений с неполярными и слабополярными связями.
Такие связи (например, C–C, C–H, Cl–Cl, O–O и т.п.) склонны к гомолитическому разрыву.

Условия проведения радикальных реакций:
- повышенная температура (часто реакцию проводят в газовой фазе),
- действие света или радиоактивного излучения,
- присутствие соединений – источников свободных радикалов (инициаторов), например, пероксидов ROOR.
- неполярные растворители.








