Нуклеофильные реакции
Нуклеофильной называется реакция, в которой молекула органического вещества подвергается действию нуклеофильного реагента.
Нуклеофильные ("любящие ядро") реагенты, или нуклеофилы — это частицы (анионы или молекулы), имеющие неподеленную пару электронов на внешнем электронном уровне.
Примеры нуклеофильных частиц: OH–, Cl–, Br–, CN–, H2O, CH3OH, NH3.
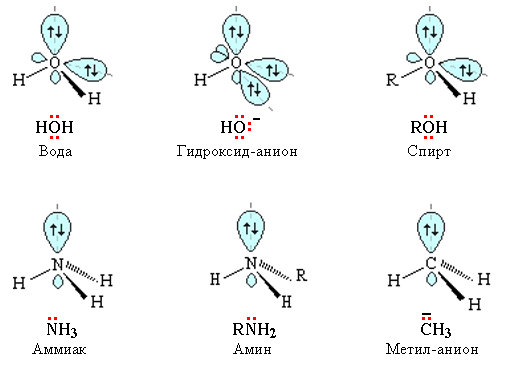
Нуклеофильное замещение:
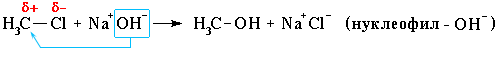
Анимация
Механизм нуклеофильного замещения обозначается символом SN
(по первым буквам английских терминов: S – Substitution [замещение], N – Nucleophile [нуклеофил]).
(по первым буквам английских терминов: S – Substitution [замещение], N – Nucleophile [нуклеофил]).
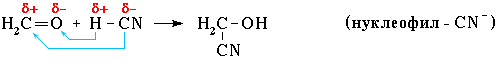
Обозначение механизма: AdN (Ad – Addition [присоединение]).








