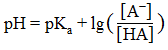Кислотные свойства карбоновых кислот
Карбоновые кислоты значительно превосходят по кислотности спирты ROH и фенолы ArOH. В водном растворе карбоновые кислоты диссоциируют на ионы:
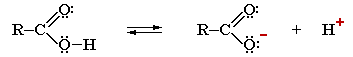
или
R–COOH + H2O 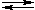 R–COO– + H3O+
R–COO– + H3O+
Кислая среда обнаруживается с помощью индикаторов.
Степень диссоциации зависит от устойчивости анионов RCOO
– (карбоксилат-ионов). Эти анионы стабильнее (и легче образуются), чем соответствующие спиртам и фенолам анионы RO
– и ArO
–. Причина большей устойчивости карбоксилат-ионов — равномерное распределение (делокализация) отрицательного заряда между двумя атомами кислорода:
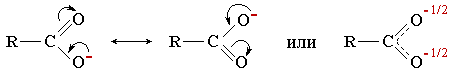
Однако карбоновые кислоты в целом – слабые кислоты: в водных растворах их соли сильно гидролизованы.
 Видеоопыт
Видеоопыт "Карбоновые кислоты – слабые электролиты".
Сила кислот зависит от строения радикала. Электроноакцепторные заместители в радикале усиливают кислотность. Так, в ряду хлоруксусных кислот их сила возрастает с увеличением количества электроотрицательных атомов хлора:

Электронодонорные заместители, напротив, уменьшают кислотные свойства карбоксила. Поэтому пропионовая кислота CH
3CH
2COOH и последующие гомологи слабее уксусной кислоты, а самой сильной в гомологическом ряду одноосновных кислот является муравьиная кислота
H–COOH.
Константы кислотности pKa* некоторых кислот в воде при 25 °С
| Кислота | pKa | Кислота | pKa |
| HCOOH | 3,75 | СН2ClCOOH | 2,86 |
| CH3COOH | 4,74 | CHCl2COOH | 1,26 |
| CH3CH2COOH | 4,87 | CCl3COOH | 0,64 |
| C6H5COOH | 4,20 | CF3COOH | 0,23 |
| H2O | 15,7 | HCl | –7 |
* Значение pH связано с pKa соотношением: 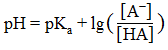
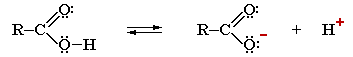
 R–COO– + H3O+
R–COO– + H3O+
 Видеоопыт "Карбоновые кислоты – слабые электролиты".
Видеоопыт "Карбоновые кислоты – слабые электролиты".