Карбонильная группа C=O влияет на связанный с ней углеводородный радикал, проявляя свойства электроноакцепторного Электроноакцепторный заместитель – группа атомов (или атом), которая пони-жает электронную плотность (увеличи-вает положительный заряд) на связанном с нею углеводородном фрагменте. заместителя.
В зависимости от природы радикала альдегиды и кетоны могут вступать в реакции:
-
- замещения атома водорода в предельногом радикале при разрыве связи С–Н, ближайшей к группе С=О, то есть в α-СН-звене;
- замещения водорода в бензольном кольце ароматического радикала;
- присоединения по кратной углерод-углеродной связи непредельного радикала.
Предельные альдегиды и кетоны способны к замещению атома водорода в α-СН-звене. Эти реакции характерны для соединений, в которых группа С=О находится при sp3-атоме углерода алкильного радикала: метильного (-CH3), первичного (-CH2R) или вторичного (-CHR2). Третичные радикалы (-CR3) не содержат подвижного атома водорода и в этих реакциях не участвуют.
Под влиянием –I-эффекта карбонильной группы в молекуле альдегида (или кетона) повышается полярность связи С–Н в α-положении (соседнем с группой С=О). Это увеличивает подвижность атома водорода и способствует его замещению.

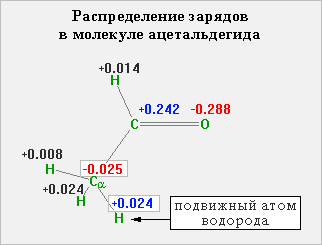
Распределение зарядов в молекуле ацетальдегида
- Галогенирование. Реакции замещения α-атома водорода на галоген (Cl, Br, I) протекают легко в присутствии кислот или оснований:

Механизм реакции
 Карбонильные соединения, в которых карбонил связан с метильной группой (-СОCH3), вступают в галоформную реакцию. При действии иода в щелочной среде (йодоформная реакция) образуется осадок иодоформа CHI3 желтого цвета.
Карбонильные соединения, в которых карбонил связан с метильной группой (-СОCH3), вступают в галоформную реакцию. При действии иода в щелочной среде (йодоформная реакция) образуется осадок иодоформа CHI3 желтого цвета.CH3–CO–CH3 + 3I2 + 4NaOH → CH3–COONa + CHI3↓ + 3H2O + 3NaI Эта реакция является качественной для определения метилкетонов и ацетальдегида, а также для этанола, окисляемого йодом в ацетальдегид, и спиртов, содержащих фрагмент -С(ОН)CH3, который в условиях реакции окисляется до группы -СОСН3. Видеоопыт "Взаимодействие ацетона с йодом".
Механизм галоформной реакции.
Представители галоформов: хлороформХлороформ – легкокипящая жидкость, обладает сильным наркотическим действием. В настоящее время исполь-зование хлороформа для наркоза в медицине ограничено из-за его срав-нительно высокой токсичности. CHCl3, иодоформИодоформ – твердое вещество желтоватого цвета с резким характерным запахом. Плохо растворим в спирте, эфире, хлороформе, практически нераст-ворим в воде. В медицине применяется как наружное антисептическое средство в виде мазей и присыпок. CHI3.
Видеоопыт "Взаимодействие ацетона с йодом".
Механизм галоформной реакции.
Представители галоформов: хлороформХлороформ – легкокипящая жидкость, обладает сильным наркотическим действием. В настоящее время исполь-зование хлороформа для наркоза в медицине ограничено из-за его срав-нительно высокой токсичности. CHCl3, иодоформИодоформ – твердое вещество желтоватого цвета с резким характерным запахом. Плохо растворим в спирте, эфире, хлороформе, практически нераст-ворим в воде. В медицине применяется как наружное антисептическое средство в виде мазей и присыпок. CHI3. Реакции конденсации с участием α-СН–звена. См. Альдольно-кротоновая конденсация.

Непредельные карбонильные соединения способны к реакциям присоединения по кратным углерод-углеродным связям в углеводородном радикале.
Наибольшее влияние на эти реакции оказывает группа C=O, если она находится в сопряжении со связью С=С (например,

В этом случае карбонильное соединение может вступать в реакцию с реагентом HX по типу 1,4-присоединения (подобно сопряженным диенам). Образующийся при этом неустойчивый непредельный спирт (енол) изомеризуется в карбонильное соединение. Таким образом, результатом реакции является продукт присоединения по связи С=С против правила Марковникова. Пример:









