Реакции дегидратации спиртов
Отщепление воды от молекул спирта (дегидратация спиртов) происходит при действии концентрированной серной кислоты и в зависимости от температуры может идти как внутримолекулярная или межмолекулярная реакция.
- Внутримолекулярная дегидратация спиртов осуществляется при повышенной температуре и приводит к образованию алкенов (реакция элиминирования):
- Межмолекулярная дегидратация спиртов с образованием простых эфиров происходит при более низкой температуре, чем внутримолекулярная реакция:
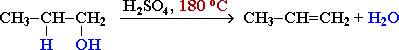

дегидратация идет преимущественно в направлении I, то есть по правилу Зайцева
– с образованием более замещённого алкена (водород отщепляется от менее гидрогенизированного атома углерода).
Легкость внутримолекулярной дегидратации спиртов уменьшается в ряду:

Активность спиртов при межмолекулярной дегидратации:








