Получение спиртов и фенолов
1. Метанол в промышленности получают из синтез-газаПаровая конверсия метана , катализаторы – оксиды Zn, Cr, Al:
, катализаторы – оксиды Zn, Cr, Al:
 CH2OH
CH2OH- а) ферментативное брожение глюкозы C6H12O6, полученной из пищевого сырья (зерновых культур, картофеля) или отходов сахарного производства по схеме:
в) гидратация этилена (синтетический спирт)
(CH3)2C=CH2 + H2O (Н+) → (CH3)3C–OH
ClCH2–CH2Cl + 2 NaOH (водн.) → HOCH2–CH2OH + 2NaCl
C6H5Cl + NaOH (p, 340 °С) → C6H5OH + NaCl
R2C=O + H2 (Ni) → R2CH–OH (вторичные спирты)
Реактивы Гриньяра – алкилмагнийгалогениды R–MgHal – смешанные магниевые соли галогеноводородных кислот HHal и алканов RH, получаемые при взаимодействии магния с алкилгалогенидом RHal в среде безводного эфира. Реактивы Гриньяра служат источниками карбанионов R:–, являющихся сильными нуклеофилами и основаниями.
- Присоединение R-MgHal к формальдегиду приводит к образованию первичных спиртов:
- Из альдегидов получаются вторичные спирты:
- В реакции с кетонами образуются третичные спирты:
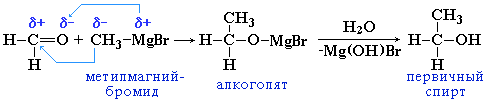
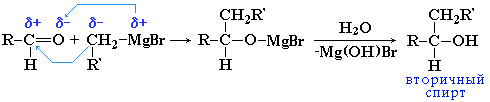
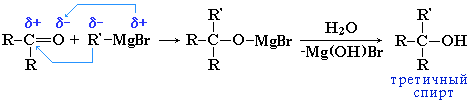
7. Гликоли получают окислением алкенов щелочным раствором KMnO4 (реакция Вагнера):

8. Кумольный метод получения фенола (совместно с ацетоном) занимает ведущее место в мировом промышленном производстве.
Основой метода являются реакции, открытые советским химиком Р.Ю. Удрисом (1942 г.):
• жидкофазное окисление кумола (изопропилбензола) кислородом воздуха до гидропероксида,
• кислотное гидролитическое расщепление гидропероксида кумола на фенол и ацетон.

Технологический процесс получения фенола и ацетона из бензола и пропилена через кумол (кумольный метод) разработан Р.Ю. Удрисом, П.Г. Сергеевым, Б.Д. Кружаловым и М.С. Немцовым (1942-1946).
Подробнее
В 1949 году в г. Дзержинске впервые в мире была запущена промышленная установка, реализующая этот процесс.
Преимущества кумольного метода: безотходная технология (выход полезных продуктов > 99%) и экономичность. В настоящее время этот метод является основным в мировом производстве фенола. Важное место кумольный метод занял в технологии современных крупнотоннажных производств эпоксидных смол и поликарбонатов, где используется продукт конденсации фенола с ацетоном (реакция Дианина) — бисфенол А (дианДиан – название бисфенола А, данное в честь русского химика Александра Дианина, впервые получившего это соединение (1891 г.).).
(дианДиан – название бисфенола А, данное в честь русского химика Александра Дианина, впервые получившего это соединение (1891 г.).).
9. Фенол и крезолы извлекают из каменноугольной смолы.
Кумольный метод совместного получения фенола и ацетона
1. Синтез гидропероксида кумола

2. Кислотное расщепление гидропероксида кумола

1. Синтез гидропероксида кумола

2. Кислотное расщепление гидропероксида кумола

 (дианДиан – название бисфенола А, данное в честь русского химика Александра Дианина, впервые получившего это соединение (1891 г.).).
(дианДиан – название бисфенола А, данное в честь русского химика Александра Дианина, впервые получившего это соединение (1891 г.).).







 Фрацузский химик-органик, член Парижской АН (с 1926). Ученик Ф.А. Барбье. Родился в Шербуре. Окончил Лионский университет (1893). В 1900-1909 работал там же, с 1909 - в университете Нанси (с 1910 профессор). В годы первой мировой войны - в военно-химической лаборатории в Сорбонне. В 1917-1918 читал лекции в Милонском институте (США). В 1919-1935 вновь в Лионском университете, с 1921 одновременно директор Школы химической промышленности в Лионе. Основатель 23-томного издания "Руководство по органической химии". Член ряда Академий наук и научных обществ. Лауреат Нобелевской премии (1912).
Фрацузский химик-органик, член Парижской АН (с 1926). Ученик Ф.А. Барбье. Родился в Шербуре. Окончил Лионский университет (1893). В 1900-1909 работал там же, с 1909 - в университете Нанси (с 1910 профессор). В годы первой мировой войны - в военно-химической лаборатории в Сорбонне. В 1917-1918 читал лекции в Милонском институте (США). В 1919-1935 вновь в Лионском университете, с 1921 одновременно директор Школы химической промышленности в Лионе. Основатель 23-томного издания "Руководство по органической химии". Член ряда Академий наук и научных обществ. Лауреат Нобелевской премии (1912).
