Восстановление альдегидов и кетонов
Присоединение водорода по карбонильной группе в присутствии Ni-катализатора приводит к восстановлению альдегидов до первичных спиртов, а кетонов – до вторичных: 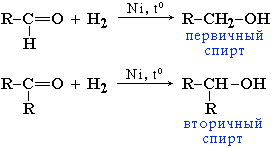
При этом степень окисления карбонильного атома углерода понижается в реакции с альдегидом от +1 до –1, а в реакции с кетоном – от +2 до 0.
Исключение составляет восстановление муравьиного альдегида H2C=O до метилового спирта CH3OH. В этом случае степень окисления углерода изменяется от
В лабораторных условиях для восстановления альдегидов и кетонов используется алюмогидрид лития LiAlH4.
Альдегиды, у которых отсутствует подвижный атом водорода в α-положении, при действии концентрированного раствора щелочи подвергаются диспропорционированию (реакция Канниццаро): половина всего количества альдегида восстанавливается до спирта, а другая – окисляется в карбоновую кислоту, выделяющуюся в виде соли:
2C6H5CH=O + KOH → C6H5CH2OH + C6H5COOK








