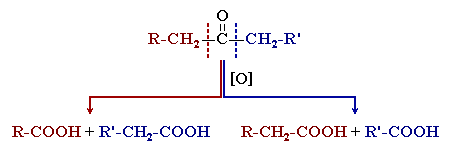
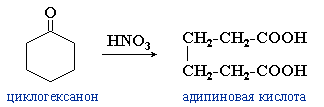
Реакции окисления альдегидов и кетонов
Альдегиды и кетоны резко отличаются по способности к окислению.Если реакция проводится в щелочной среде, карбоновая кислота образуется в виде соли, например: R–СОО–NH4+.
- Реакция "серебрянного зеркала" – окисление аммиачным раствором оксида серебра
Ag2O + 4NH4OH
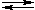 2[Ag(NH3)2]OH + 3H2O
(реактив Толленса):
2[Ag(NH3)2]OH + 3H2O
(реактив Толленса):
R–CH=O + 2[Ag(NH3)2]OH  RCOO–NH4+ + 2Ag↓ + 3NH3↑ + H2O
RCOO–NH4+ + 2Ag↓ + 3NH3↑ + H2O - Окисление гидроксидом меди (II):
а) в виде свежеприготовленного осадка Cu(OH)2 при нагревании,
б) в форме комплекса с аммиаком [Cu(NH3)4](OH)2,
в) в составе комплекса с солью винной кислоты (реактив Фелинга).
При этом образуется красно-кирпичный осадок оксида меди (I) или металлическая медь (реакция "медного зеркала", более характерная для формальдегида):
R-CH=О + 2Cu(OH)2  RCOOH + Cu2O↓ + H2О
RCOOH + Cu2O↓ + H2О
H2C=О + Cu(OH)2  HCOOH + Cu↓ + H2О
HCOOH + Cu↓ + H2О
R–CH=O + 2[Cu(NH3)4](OH)2  RCOO–NH4+ + Cu2O↓ + 3NH3↑ + 2H2O
RCOO–NH4+ + Cu2O↓ + 3NH3↑ + 2H2O
R–CH=OВ данную реакцию ароматические альдегиды не вступают. + 2Cu(OH)2/соль винной кислоты RCOOH + Cu2O↓ + 2H2O
RCOOH + Cu2O↓ + 2H2O
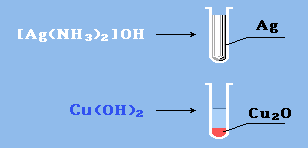
Данные реакции являются качественными на альдегидную группу.
 Видеоопыт "Качественная реакция на альдегиды с гидроксидом меди (II)"
Видеоопыт "Качественная реакция на альдегиды с гидроксидом меди (II)"
 Видеоопыт "Реакция серебрянного зеркала"
Видеоопыт "Реакция серебрянного зеркала"
 Видеоопыт "Качественная реакция с
фуксинсернистой кислотой"
Видеоопыт "Качественная реакция с
фуксинсернистой кислотой"