Крекинг алканов
Крекингот англ. cracking - расщепление
– процесс термического разложения углеводородов, в основе которого лежат реакции расщепления углеродной цепи крупных молекул с образованием соединений с более короткой цепью.
Крекинг алканов является основой переработки нефти с целью получения продуктов меньшей молекулярной массы, которые используются в качестве моторных топлив, смазочных масел и т.п., а также сырья для химической и нефтехимической промышленности.Для осуществления этого процесса используются два способа: термический крекинг (при нагревании без доступа воздуха и повышенном давлении) и каталитический крекинг (более умеренное нагревание в присутствии катализатора). Термический крекинг. При температуре 480–550 °С и давлении 5 МПа алканы распадаются за счет разрыва связей
Например:

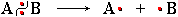
Гомолитический разрыв
ковалентной связи

Свободные радикалы очень активны. Один из них (например, этил) отщепляет атомарный водород Н• от другого (н-бутила) и превращается в алкан (этан). Другой радикал, став двухвалентным, превращается в алкен (бутен-1) за счет образования π–связи при спаривании двух электронов у соседних атомов:

Анимация
(работа Литвишко Алексея, ученика 9 кл. школы №124 г. Самары)

В общем виде этот процесс можно выразить схемой:
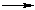 CmH2m + CpH2p+2,
где m + p = n
CmH2m + CpH2p+2,
где m + p = n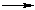 C + 2H2
C + 2H2-
Пример:
крекинг н-октана с образованием изобутана и изобутена (работа Литвишко Алексея, ученика 9 кл. школы №124 г. Самары).
Реакции изомеризации н-алканов приводят к разветвленным структурам. При дегидрировании алканов образуются циклические углеводороды (реакция дегидроциклизации). Наличие в составе бензина разветвлённых и циклических углеводородов повышает его качество – детонационную устойчивость, выражаемую октановым числом.
Октановое число — условная количественная характеристика детонационной стойкостиДетонационная стойкость — способность противостоять самовоспламенению при сжатии. моторных топлив, применяемых в карбюраторных двигателях внутреннего сгорания. Октановое число численно равно процентному (по объему) содержанию изооктана (2,2,4-триметилпентана), октановое число которого принято за 100, в его смеси с н-гептаном (октановое число равно 0), эквивалентной по детонационной стойкости испытуемому топливу при стандартных условиях испытания.
При крекинг-процессах образуется большое количество газов, которые содержат главным образом предельные и непредельные углеводороды. Эти газы используются в качестве сырья для химической промышленности.
Основополагающие работы по каталитическому крекингу в присутствии хлорида алюминия проведены
- Видео "Каталитический крекинг нефти"








