АРЕНЫ
Арены (ароматические углеводороды) — группа углеводородов, молекулы которых содержат устойчивые циклические группы атомов (бензольные кольца) с замкнутой системой сопряжённых (делокализованных) связей.
с замкнутой системой сопряжённых (делокализованных) связей.
По числу бензольных колец (бензольных ядер) в структуре молекул арены подразделяются на моноядерные (одноядерные) и полиядерные (многоядерные).
 с замкнутой системой сопряжённых (делокализованных) связей.
с замкнутой системой сопряжённых (делокализованных) связей.В приведённых ниже примерах использованы тривиальные названия аренов, принятые в номенклатуре ИЮПАК (бензол, толуол, стирол, нафталин и др.).
• Моноядерные арены — моноциклические соединения, содержащие в молекуле одно бензольное кольцо.

Модели молекул

- Известные моноядерные арены:
ксилол
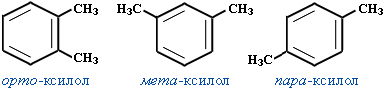 ы – изомеры C6H4(CH3)2,
ы – изомеры C6H4(CH3)2,
 C6H5CH(CH3)2,
C6H5CH(CH3)2, C6H5–CH=CH2,
C6H5–CH=CH2, C6H3(CH3)3.
C6H3(CH3)3.
В зависимости от типа связывания бензольных ядер в молекулах полиаренов различают:
- конденсированные ароматические углеводороды, бензольные кольца которых имеют общие атомы углерода (нафталин,
антрацен, фенантрен);Антрацен и фенантрен — изомеры, отличающиеся способом связывания (сочленения) бензольных колец:
антрацен — линейно сочленённый изомер.
фенантрен — ангулярно сочленённый (от лат. angulus — угол, угловой). - полиарены, содержащие бензольные кольца, соединенные простой σ-связью (дифенил);
- ди- и полиарилалканы, в молекулах которых кольца разделены алкильной группой (дифенилметан).
Ароматичность означает повышенную устойчивость циклических молекул с замкнутой π-электронной системой сопряжения.
Устойчивость ароматических соединений проявляется в их инертности при реакциях, приводящих к нарушению циклической системы сопряжения (ароматической структуры). Несмотря на формальную ненасыщенность бензольного кольца, арены не склонны к реакциям присоединения, сопровождающиxся утратой ароматичности.
Ароматический характер аренов объясняется электронным строением бензольного кольца (см. далее).








