Замещение в алкилбензолах
Гомологи бензола (алкилбензолы) более активно вступают в реакции электрофильного замещения (SE) по сравнению с бензолом.
Например, при нитровании толуола С6Н5CH3 в мягких условиях (20-30 °C) замещается один атом водорода с образованием смеси изомерных 2- и 4-нитротолуолов
 При повышении температуры и концентрации нитрующей смеси замещаются два атома водорода и получают 2,4- и 2,6-динитротолуолы.
При повышении температуры и концентрации нитрующей смеси замещаются два атома водорода и получают 2,4- и 2,6-динитротолуолы. Нитрование в ещё более жестких условиях приводит к превращению обоих изомерных динитротолуолов в 2,4,6-тринитротолуол (тротилТротил (тол, 2,4,6-тринитротолуол) — известное взрывчатое вещество. Взрывается только от детонации. Горит коптящим пламенем без взрыва. Мощность любых взрывчатых устройств принято измерять в тротиловом эквиваленте.):
Нитрование в ещё более жестких условиях приводит к превращению обоих изомерных динитротолуолов в 2,4,6-тринитротолуол (тротилТротил (тол, 2,4,6-тринитротолуол) — известное взрывчатое вещество. Взрывается только от детонации. Горит коптящим пламенем без взрыва. Мощность любых взрывчатых устройств принято измерять в тротиловом эквиваленте.):

В отличие от толуола прямое нитрование бензола до
1,3,5-тринитробензола не даёт практического результата.
не даёт практического результата.

 Нитрование в ещё более жестких условиях приводит к превращению обоих изомерных динитротолуолов в 2,4,6-тринитротолуол (тротилТротил (тол, 2,4,6-тринитротолуол) — известное взрывчатое вещество. Взрывается только от детонации. Горит коптящим пламенем без взрыва. Мощность любых взрывчатых устройств принято измерять в тротиловом эквиваленте.):
Нитрование в ещё более жестких условиях приводит к превращению обоих изомерных динитротолуолов в 2,4,6-тринитротолуол (тротилТротил (тол, 2,4,6-тринитротолуол) — известное взрывчатое вещество. Взрывается только от детонации. Горит коптящим пламенем без взрыва. Мощность любых взрывчатых устройств принято измерять в тротиловом эквиваленте.):

В отличие от толуола прямое нитрование бензола до
1,3,5-тринитробензола
 не даёт практического результата.
не даёт практического результата. Здесь ярко проявляется взаимное влияние атомов в молекуле на реакционную способность вещества.
• С одной стороны, метильная группа СH3 за счёт электронодонорного +I-эффекта повышает электронную плотность в бензольном кольце в положениях 2, 4 (орто) и 6 (пара):
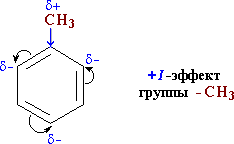
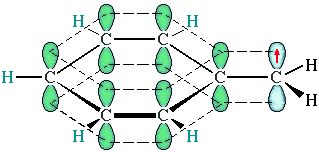
Кроме +I-эффекта важную роль играет эффект сверхсопряжения, проявляемый метильной группой СH3 и, в меньшей степени, группами CH2R и СHR2


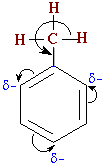
Взаимодействие электронов σ-cвязи С–Н с π-системой бензольного кольца
усиливает электронодонорные свойства метильной группы и повышает электронную плотность в орто- и пара-положениях кольца (дополнительно к +I-эффекту).
Замена атомов водорода в СH3-группе на углеводородные радикалы R ослабляет эффект сверхсопряжения в ряду:–СH3 > –CH2R > –СHR2
(в группе –CR3 сверхсопряжение отсутствует).
В противоположном порядке увеличивается +I-эффект алкильных групп:
–CR3 > –СHR2 > –CH2R > –СH3
Известно, что скорость электрофильного замещения в алкилбензолах убывает ряду:
С6Н5-CH3 > С6Н5-CH2CH3 >
С6Н5-CH(CH3)2 > С6Н5-C(CH3)3 > С6Н5-H
Данный ряд совпадает с порядком ослабления эффекта сверхсопряжения алкильных групп.
Из этого следует, что cверхсопряжение вносит более существенный вклад в стабилизацию промежуточных карбокатионов (σ-комплексов), образующихся на лимитирующей стадии, которая определяет общую скорость реакции (часть I. Роль промежуточных частиц). Устойчивость σ-комплекса тем выше, чем в большей степени делокализован его заряд. Дополнительный вклад в стабилизацию σ-комплексов вносит эффект сверхсопряжения:

Делокализация заряда в промежуточных ионах
с участием σ-электронов связи С–Н.
В общем случае реакционная способность производных бензола С6Н5X и направление электрофильного замещения определяются правилами ориентации.
- Cверхсопряжение (гиперконъюгация) — слабый эффект делокализации электронов σ-cвязи С–Н, находящейся при sp2 или sp-атоме.


Замена атомов водорода в СH3-группе на углеводородные радикалы R ослабляет эффект сверхсопряжения в ряду:
(в группе –CR3 сверхсопряжение отсутствует).

Делокализация заряда в промежуточных ионах
с участием σ-электронов связи С–Н.
В общем случае реакционная способность производных бензола С6Н5X и направление электрофильного замещения определяются правилами ориентации.
• С другой стороны, под влиянием бензольного кольца метильная группа СH3 в толуоле становится более активной в реакциях радикального замещения (SR) по сравнению с метаном СH4 и другими алканами (Алканы. Реакции замещения). Например, скорость замещения водорода бромом в метильной группе толуола в 108 выше, чем водорода в метане.
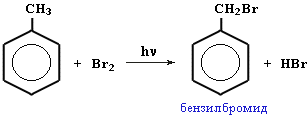
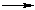 C6H5-ĊH2 + HBr
C6H5-ĊH2 + HBrCH4 + •Br
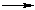 ĊH3 + HBr
ĊH3 + HBr