Строение двойной связи С=С
Двойная связь C=C является сочетанием σ- и π-связей.
Хотя эта связь изображается двумя одинаковыми черточками "=", всегда следует учитывать их неравноценность. σ-Связь возникает при осевом перекрывании sp
2-гибридных орбиталей, а π-связь – при боковом перекрывании р-орбиталей соседних sp
2-гибридизованных атомов углерода
(часть I, Форма σ- и π-МО). Образование связей в молекуле этилена можно изобразить следующей схемой:
С=С σ-связь (перекрывание 2sp2↔2sp2) + π-связь (2рz↔2рz);
С–Н σ-связь (перекрывание 2sp2-АО углерода ↔ 1s-АО водорода).
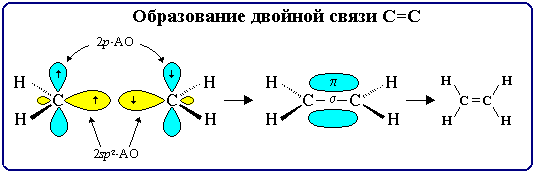
σ-Связи, образуемые sp
2-гибридными орбиталями, находятся в одной плоскости под углом 120°. Поэтому молекула этилена имеет плоское строение (все атомы лежат в одной плоскости). Условная плоскость π-связи перпендикулярна плоскости молекулы, так как угол между sp
2-АО и р-АО равен 90°:
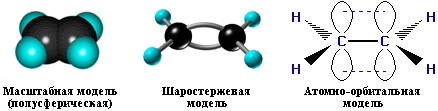
 Модели молекулы этилена
Модели молекулы этилена
Анимация
VRML-модель
По своей природе π-связь резко отличается от σ-связи: π-связь менее прочная вследствие меньшей эффективности перекрывания р-орбиталей.
В молекуле пропилена
СН2=СН–СН3 в одной плоскости лежат
6 атомов: два sp
2-атома углерода и четыре связанные с ними атома (3 атома Н и атом С группы СН
3).
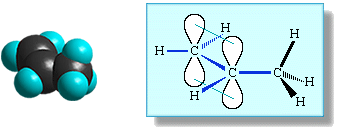
Один из атомов водорода метильной группы СН
3, имеющей тетраэдрическое строение, также может находиться в этой плоскости за счёт внутримолекулярного вращения по связи
Csp2–Csp3, например, в
заслоненной конформации
, стабилизированной взаимодействием π-МО двойной связи и σ-МО связи C
sp3–Н.
Аналогичное строение имеют и другие алкены.

 Модели молекулы этилена
Модели молекулы этилена


 , стабилизированной взаимодействием π-МО двойной связи и σ-МО связи Csp3–Н.
Аналогичное строение имеют и другие алкены.
, стабилизированной взаимодействием π-МО двойной связи и σ-МО связи Csp3–Н.
Аналогичное строение имеют и другие алкены.








