Гидрирование (присоединение водорода)
При взаимодействии бутадиена-1,3 с водородом в момент выделения (например, в реакции натрия со спиртомC2H5OH + Na• → C2H5O–Na+ + H•) получается бутен-2, то есть происходит 1,4-присоединение. Формально этот процесс можно представить следующим образом: при действии реагента двойные связи разрываются, к крайним атомам углерода С(1) и С(4) присоединяются атомы водорода (H•), а свободные валентности (неспаренные электроны) образуют π-связь между атомами С(2) и С(3):

 (н-бутан)
(н-бутан)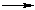 (CH3)2C=CH–CH3 (2-метилбутен-2)
(CH3)2C=CH–CH3 (2-метилбутен-2) CH2=С(CH3)–CH=CH2 + 2H2 (Ni, t)
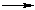 (CH3)2CH–CH2–CH3 (2-метилбутан)
(CH3)2CH–CH2–CH3 (2-метилбутан)Галогенирование (присоединение галогенов)
Хлор и бром легко присоединяются к алкадиенам по электрофильному механизмуЭлектрофильный механизм характерен для реакций, в которых молекула органического вещества подвергается действию электрофильного реагента (электрофила) – частицы (катиона или молекулы), имеющей свободную орбиталь на внешнем электронном уровне и способной принять пару электронов при образовании ковалентной связи по донорно-акцепторному механизму. подобно алкенам.
При взаимодействии эквимолярных количеств бутадиена-1,3 и брома образуются продукты как 1,2-, так и 1,4-присоединения:

 (при 1,2-присоединении) более стабильны и поэтому легче образуются, чем первичные
(при 1,2-присоединении) более стабильны и поэтому легче образуются, чем первичные  (при 1,4-присоединении). Повышение температуры реакции смещает равновесие в сторону образования более термодинамически устойчивыхЧем больше заместителей при двойной связи, тем выше термодинамическая стабильность вещества:
(при 1,4-присоединении). Повышение температуры реакции смещает равновесие в сторону образования более термодинамически устойчивыхЧем больше заместителей при двойной связи, тем выше термодинамическая стабильность вещества:Следует отметить, что 1,4-присоединение реагентов (кроме водорода) к бутадиену-1,3 приводит к образованию смеси цис- и транс-изомеров (например, изомеры 1,4-дибромбутена-2
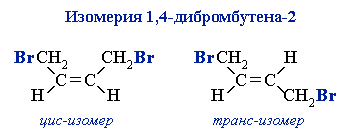 ).
).В избытке брома присоединяется еще одна его молекула по месту оставшейся двойной связи с образованием 1,2,3,4-тетрабромбутана1,2,3,4-Тетрабромбутан образуется в этой реакции в виде смеси стереоизомеров, так как в молекуле содержатся два асимметрических атома углерода: С(2) и С(3).:
 CH2=С(CH3)–CHBr–CH2Br
CH2=С(CH3)–CHBr–CH2Br
Гидрогалогенирование (присоединение галогеноводородов)
Присоединение HCl и HBr к сопряженным диенам происходит также в 1,2- (3,4-) и 1,4-положения и подчиняется тем же закономерностям: с повышением температуры увеличивается доля продукта 1,4-присоединения.

1,4-присоединение - термодинамически контролируемая реакция.
Присоединение воды и других полярных реагентов происходит по электрофильному механизму (как в алкенах). В реакциях несимметричных соединений соблюдается правило Марковникова.
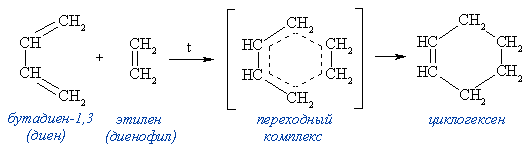
В органическом синтезе широко применяется реакция присоединения к сопряженным диенам соединений, содержащих кратные связи (так называемых диенофилов). Реакция идет как 1,4-присоединение и приводит к образованию циклического продукта (такие реакции называют реакциями циклоприсоединения):