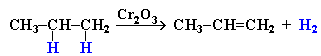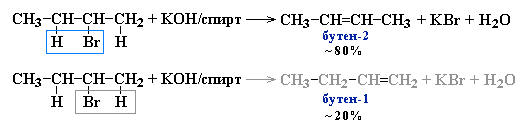Получение алкенов
В природе алкены встречаются в значительно меньшей степени, чем предельные углеводороды, по-видимому, вследствие своей высокой реакционной способности. Поэтому их получают с использованием различных реакций.
I. Крекинг алканов:
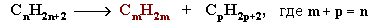
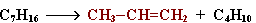
II. Отщепление (элиминирование) двух атомов или групп атомов от соседних атомов углерода с образованием между ними π-связи.
- Дегидрогалогенирование галогеналканов при действии спиртового раствора щелочи
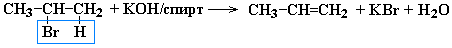
Почему для дегидрогалогенирования используется раствор щелочи в спирте, а не в воде?
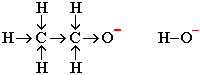
В растворе КОН (или NaOH) в этиловом спирте С2Н5ОН присутствуют ионыС2Н5О–, которые образуются в результате реакции: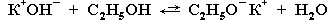
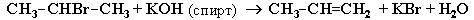
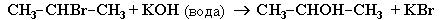
- Дегидратация спиртов при повышенной температуре (выше 140 °C)
в присутствии водоотнимающих реагентов
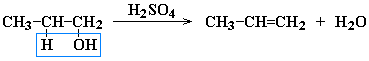
Реакции элиминирования идут в соответствии с правилом Зайцева:
Отщепление атома водорода в реакциях дегидрогалогенирования и дегидратации происходит преимущественно от наименее гидрогенизированного атома углерода.Современная формулировка:Реакции отщепления идут с образованием более замещенных при двойной связи алкенов
(такие алкены обладают более низкой энергией). - Дегалогенирование дигалогеналканов, имеющих атомы галогена у соседних атомов углерода, при действии активных металлов :
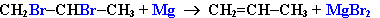
- Дегидрирование алканов при 500 °С: