и meros — часть. эффектом или эффектом сопряжения.
По направлению смещения электронной плотности различают положительный (+М) и отрицательный (–М) эффекты заместителей. Знак М-эффекта зависит от природы заместителя и способа его сопряжения с π-системой.

Примеры

+М-эффект характерен для заместителей, повышающих электронную плотность в сопряжённой системе. К ним относятся электронодонорные группы, которые содержат атом с неподелённой электронной парой, способный её передать в общую систему сопряжения. Такими группами являются:
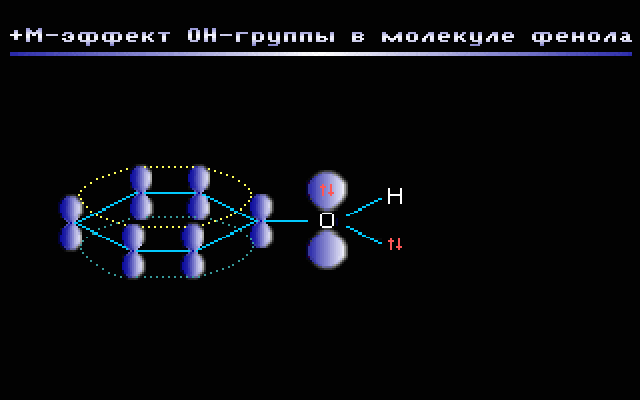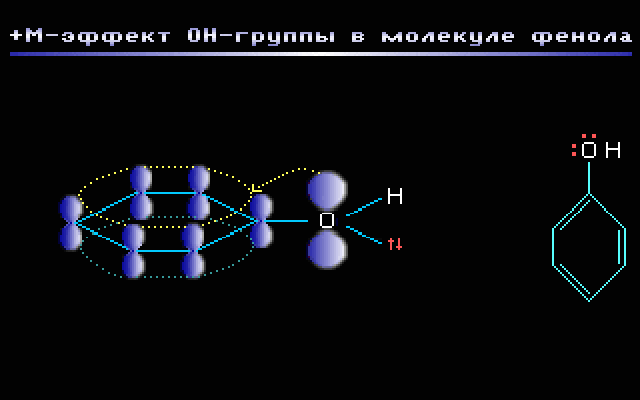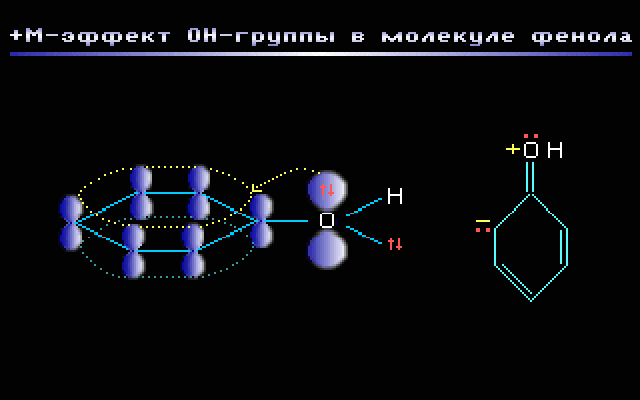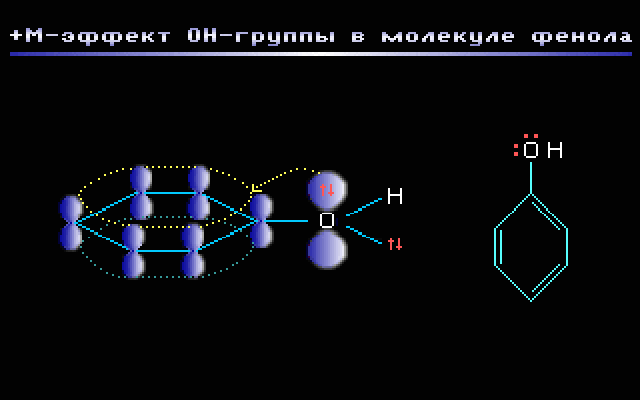
Пример. Группа –OH в молекуле фенола C6H5OH проявляет +М-эффект за счёт участия одной из неподелённых электронных пар sp2-атома кислорода в системе сопряжения. Как показано на АО-модели, это обусловлено перекрыванием негибридизованной p-орбитали атома кислорода, содержащей электронную пару, с π-системой бензольного кольца (p,π-сопряжение).

Анимация
–М-эффект проявляют заместители, содержащие электроотрицательные атомы и понижающие электронную плотность в сопряженной системе. Такими свойствами обладают электроноакцепторные группы: >C=O,  и т.п. В катионах типа
и т.п. В катионах типа  М-эффект отсутствует, так как положительно заряженный sp3-атом азота не имеет p-орбитали (АО-модель).
М-эффект отсутствует, так как положительно заряженный sp3-атом азота не имеет p-орбитали (АО-модель).
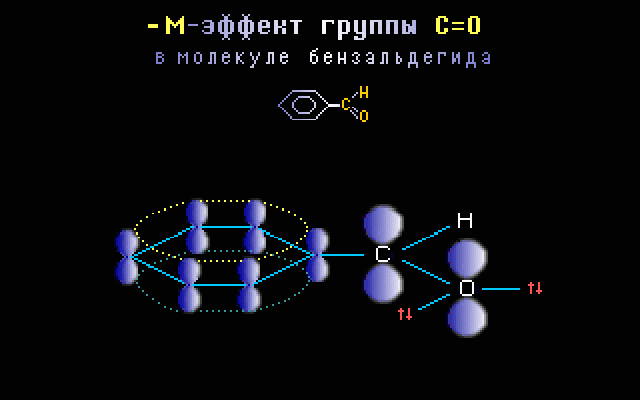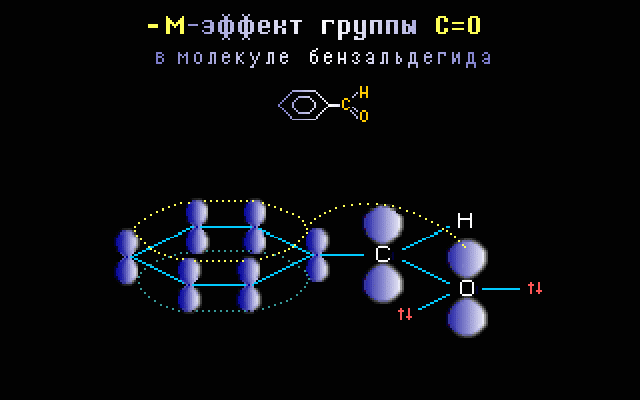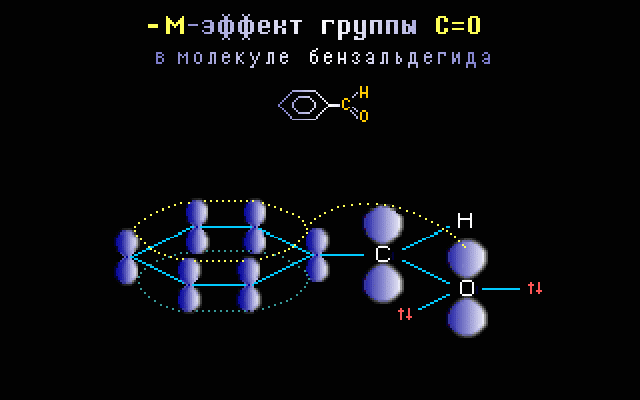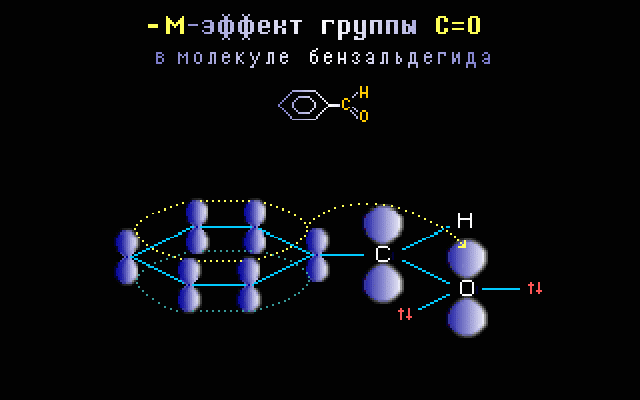
Пример. Для группы С=О в бензальдегиде C6H5CH=O характерен –М-эффект, что объясняется смещением электронов в сторону электроотрицательного атома кислорода при перекрывании

Анимация
- Величина М-эффекта растет с увеличением заряда заместителя. Ионы проявляют поэтому наиболее сильный М-эффект:
- –М-эффект заместителей тем сильнее, чем больше электроотрицательность имеющихся в заместителе элементов:
- –М-эффект заместителей тем сильнее, чем меньше их внутренняя мезомерия (делокализация электронов), например:
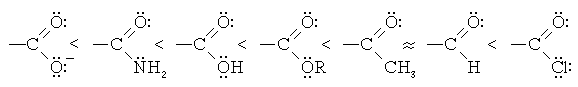
- +М-эффект заместителя тем сильнее, чем меньше электроотрицательность гетероатома, входящего в его состав:

-C≡CR < -C≡N < -NO2;
-BR2 < -AlR2.


| NO2 > CN > CO > COOH | H | Br < Cl < OCH3 < OH < NH2 < O– |
| (–M) акцепторы электронов | (+M) доноры электронов |
- К разновидности положительного мезомерного эффекта относят также довольно слабое электронное взаимодействие – эффект сверхсопряжения.








