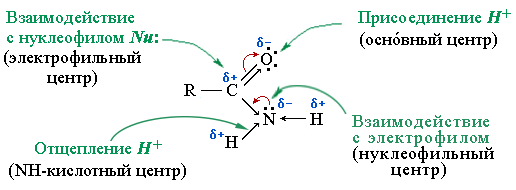
Строение амидной группы
Амидная группа 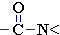 (или –C(O)N<), характер её химических связей и взаимное влияние атомов определяют физические и химические свойства амидов RCONH2, RCONHR', RCONR'2.
(или –C(O)N<), характер её химических связей и взаимное влияние атомов определяют физические и химические свойства амидов RCONH2, RCONHR', RCONR'2.
Группа -C(O)NH2 состоит из двух взаимосвязанных функциональных групп — карбонил >C=O и амино 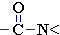 (или –C(O)N<), характер её химических связей и взаимное влияние атомов определяют физические и химические свойства амидов RCONH2, RCONHR', RCONR'2.
(или –C(O)N<), характер её химических связей и взаимное влияние атомов определяют физические и химические свойства амидов RCONH2, RCONHR', RCONR'2.
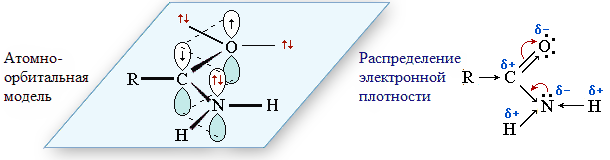
- Электронная плотность в системе O.....C.....N смещена к более электроотрицательному атому кислорода, который за счёт неподелённой электронной пары способен присоединять протон, то есть проявлять осно́вные свойства.
- Осно́вность аминогруппы в амидах ослаблена вследствие участия неподелённой пары электронов атома азота в сопряжении с карбонильной группой.
- Электронодонорный характер аминогруппы, проявляющей +М-эффект, уменьшает положительный заряд (δ+) на атоме углерода. Это ослабляет активность амидов в реакциях нуклеофильного замещения этой группы по сравнению с другими функциональными производными карбоновых кислот (сложными эфирами, галогенангидридами, ангидридами).
- Карбонильная группа >C=O как электроноакцептор (–М, –I-эффекты) увеличивает полярность связи
N–H, что придаёт кислотные свойства первичным и вторичным амидам. - За счёт неподелённой пары электронов на атоме азота амиды способны выступать в качестве нуклеофильных реагентов.
- Возможность миграции протона от азота к кислороду приводит к амид-иминольной таутомерии
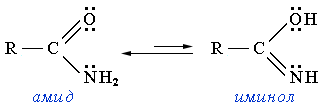 (подобно кето-енольной таутомерии).
(подобно кето-енольной таутомерии).