- Определение понятий:
• масса
Масса (m) – мера инерции тела.
Основная единица измерения массы в Международной системе единиц (СИ) – 1 кг.
Такой массой обладает 1 литр (1 дм3) дистиллированной воды при температуре
1/1000 кг = 1 г. Объем 1 г воды равен 1 мл. Соответственно, 1 м3 воды имеет массу 1000 кг или 1 т.

Электронные лабораторные весы по функционалу приближаются к персональному компьютеру и, кроме определения массы, могут выполнять расчётные операции (определение количественного состава, сложение итогов нескольких измерений, хранение информации о произведенных вычислениях, обработка, синхронизация информации и т.п.).
• объём
Единицы измерения объёма:
-
1 см3 (мл);
1 дм3 (л) = 1 000 см3 (мл) = 103 см3 (мл);
1 м3 = 1 000 дм3 (л) = 1 000 000 см3 (мл) = 106 см3 (мл).
Основная единица объёма в Международной системе единиц (СИ) — кубический метр (м3), остальные являются производными.
Объёмы жидкостей измеряют с помощью специальной (мерной) посуды: мерных цилиндров, мензурок, мерных стаканов, мерных колб, калиброванных пипеток, бюреток.

Объёмы твердых тел можно определить при погружении их в воду, измерив объём вытесненной воды с помощью мерной посуды.

• плотность
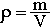 , где m – масса тела, V – его объём.
, где m – масса тела, V – его объём.Следовательно, ρ(Н2О) = 1 г/мл = 1 кг/л = 1 т/м3 (при 4 °С).
Равные объемы веществ с разной плотностью имеют разные массы. Например:
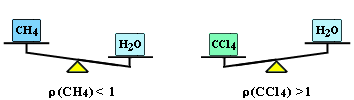
Соответственно, равные массы веществ, отличающихся плотностью, занимают разные объемы:
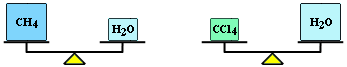
-
• закон сохранения массы веществ и энергии
• закон постоянства состава
• закон Авогадро
• закон Гесса и др.








