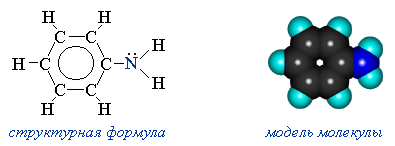
2.4. Анилин
Анилин (фениламин) С6H5NH2 – важнейший из ароматических аминов:
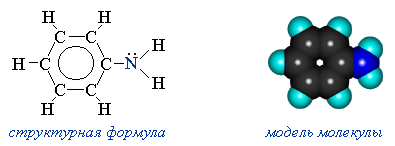
Он находит широкое применение в качестве полупродукта в производстве красителей, взрывчатых веществ и лекарственных средств (сульфаниламидные препараты).
Анилин представляет собой бесцветную маслянистую жидкость с характерным запахом (т. кип. 184 oС, т. пл. – 6 oС). На воздухе быстро окисляется и приобретает красно-бурую окраску. Ядовит.
Для анилина характерны реакции как по аминогруппе, так и по бензольному кольцу. Особенности этих реакций обусловлены взаимным влиянием атомов.
С одной стороны, бензольное кольцо ослабляет основные свойства аминогруппы по сравнению алифатическими аминами и даже с аммиаком.
С другой стороны, под влиянием аминогруппы бензольное кольцо становится более активным в реакциях замещения, чем бензол.
Например, анилин энергично реагирует с бромной водой с образованием
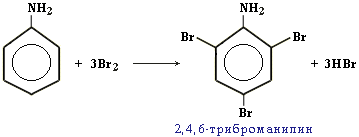
 Видеоопыт "Бромирование анилина".
Видеоопыт "Бромирование анилина".
Такое взаимное влияние атомов в молекуле анилина объясняется сопряжением
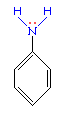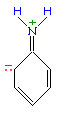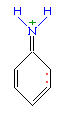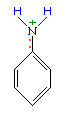
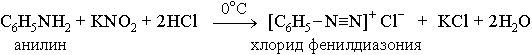
При более высокой температуре реакция идет с выделением азота и анилин превращается в фенол:
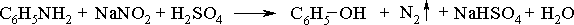
Подобно анилину реагируют с азотистой кислотой и другие первичные ароматические амины.