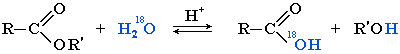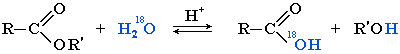Механизм реакции этерификации
Образование сложных эфиров при взаимодействии карбоновых кислот со спиртами (этерификация) происходит в условиях кислотного катализа как реакция нуклеофильного замещения гидроксильной группы Реакция включает несколько обратимых стадий.
-
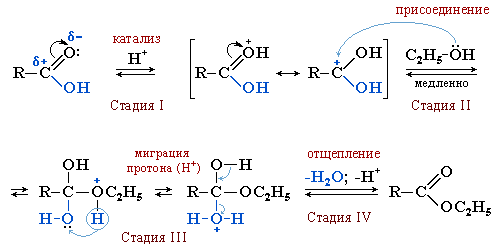
Стадия I. Активация карбоновой кислоты присоединением протона (H+) от катализатора – сильной кислоты (например, конц. H2SO4), которая превращает нейтральную молекулу в карбокатион R–C+(OH)2.
Стадия II (лимитирующая). Нуклеофильное присоединение спирта к карбокатиону. На скорость этой стадии (и реакции в целом) влияют пространственные эффекты углеводородных радикалов в молекулах спирта. Чем больше размер и число радикалов, тем выше энергия их отталкивания, определяющая энергию переходного состояния (Eакт), и тем ниже скорость реакции.
Стадия III. Миграция протона H+ и формирование хорошей уходящей группы H2O.
Стадия IV. Отщепление воды и катализатора (H+) от неустойчивого продукта присоединения с образованием cложного эфира.
Хорошей уходящей группой считается слабое основание: чем меньше основность уходящей группы, то есть её способность присоединять протон Н+, тем легче происходит отщепление. Поэтому H2O (слабое основание) — хорошая уходящая группа, а HO– (сильное основание) — плохая.
Реакционная способность спиртов при этерификации убывает с увеличением пространственных затруднений в следующем ряду:
При гидролизе сложных эфиров водой, содержащей изотоп кислорода H218O, установлено, что изотопная метка целиком оказывается в образовавшейся кислоте: