
4.4. Свойства алкенов
Физические свойства алкенов закономерно изменяются в гомологическом ряду: от С2Н4 до С4Н8 – газы, начиная с С5Н10 – жидкости, с С18Н36 – твердые вещества. Алкены практически нерастворимы в воде, но хорошо растворяются в органических растворителях.
Химические свойства алкенов определяются строением и свойствами двойной связи С=С, которая значительно активнее других связей в молекулах этих соединений. Алкены химически более активны, чем алканы.
Характеристики углерод-углеродных связей:

| Еσ+π (энергия двойной связи) С=С (σ+π) | 620 кДж/моль |
| Еσ (энергия σ-связи) С-С | 348 кДж/моль |
| Отсюда Еπ (энергия π-связи) | 272 кДж/моль, |
| т.е. Еπ на 76 кДж/моль меньше Еσ. |
Поэтому для алкенов наиболее характерны реакции, протекающие за счет раскрытия менее прочной π-связи. При этом π-связь (в исходном алкене) преобразуется в σ-связь в продукте реакции. Исходное ненасыщенное соединение превращается в насыщенное без образования других продуктов, т.е. происходит реакция присоединения.
По какому механизму идут реакции присоединения к алкенам?
1. За счет электронов π-связи в молекулах алкенов имеется область повышенной электронной плотности (облако π-электронов над и под плоскостью молекулы):
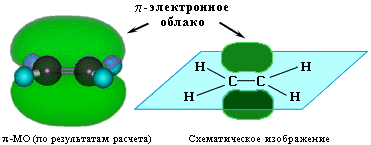
Поэтому двойная связь склонна
подвергаться атаке электрофильным (электронодефицитным) реагентом.
В этом случае будет происходить гетеролический разрыв π-связи и реакция
пойдет по ионному механизму как электрофильное присоединение.
2. С другой стороны, углерод-углеродная π-связь, являясь неполярной, может разрываться гомолитически, и тогда реакция будет идти по радикальному механизму.
Механизм присоединения зависит от условий проведения реакции.
Кроме того, алкенам свойственны реакции изомеризации и окисления (в том числе реакция горения, характерная для всех углеводородов).