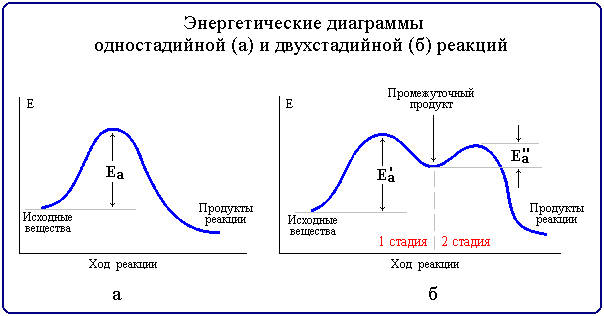
Рис. 6.3. Энергетические диаграммы
6.3. Понятие о механизме химической реакции
Механизм реакции – детальное ее описание с учетом всех промежуточных
стадий и промежуточных веществ, природы взаимодействия реагирующих
частиц, характера разрыва связей, изменения энергии химической системы
на всем пути ее перехода из исходного в конечное состояние.
Цель изучения механизма реакции – возможность управлять ходом реакции,
ее направлением и эффективностью.
Реакции, протекающие в одну стадию, называют простыми (элементарными) реакциями, а реакции, включающие несколько стадий – сложными. Энергетическая диаграмма простой реакции приведена на рис. 6.3 (а), сложной (двухстадийной) – на рис. 6.3 (б).

Многие органические реакции являются сложными и идут в несколько элементарных стадий (последовательных или параллельных). Общая скорость сложной химической реакции определяется скоростью ее наиболее медленной (лимитирующей) стадии. Например, в приведенной на рис. 6.3,б диаграмме лимитирующей является стадия 1 с более высокой энергией активации Еа'.
В случае сложных реакций на некоторых стадиях образуются нестабильные промежуточные частицы – органические ионы или свободные радикалы. Их относительная устойчивость и, следовательно, вероятность образования растут с увеличением возможности делокализации (рассредоточения) заряда в ионе или неспаренного электрона в радикале.