3.2. Основные типы химических связей
Основными типами химических связей, отличающихся друг от друга электронным строением и механизмом взаимодействия связываемых атомов, являются ковалентная и ионная связи, а также металлическая связь в металлах.
- Образование ковалентной или ионной связи в значительной степени определяется разностью электроотрицательностей (Δχ) связывемых атомов:
где χА и χВ – электроотрицательности атомов А и В.
С учётом приблизительности диапазонов значений Δχ это можно представить в виде схемы:
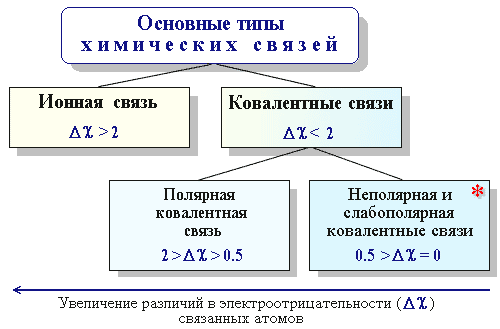
* ПримечаниеСходство свойств неполярных и слабополярных связей позволяет объединить их в одну группу.
- Металлическая связь характерна для веществ, состоящих из атомов с низкой электроотрицательностью (группа металлов).
- Таким образом, металлическая связь — это связь между положительными ионами в кристаллах металлов, осуществляемая за счет притяжения электронов, свободно перемещающихся по кристаллу.