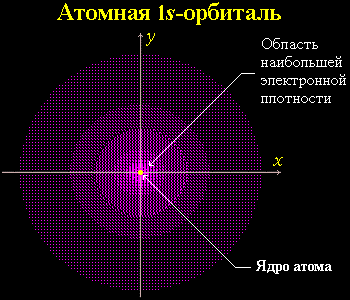
2.2.1. Свойства электрона
Электрон имеет двойственную природу. В разных экспериментах он может проявлять свойства как частицы, так и волны. Движение электрона подчиняется законам квантовой механики.Связь между волновыми и корпускулярными свойствами электрона отражает соотношение де Бройля:
-
где λ – длина волны электрона; m – его масса; v – скорость;
h = 6.62 • 10-34 Дж • с – постоянная Планка.
- Часть пространства, в котором велика вероятность нахождения электрона, называют орбиталью или электронным облаком.