2.3. Свойства аминов
Изучая новый класс соединений – амины, попробуем предсказать их основные физические и химические свойства. Для этого следует рассмотреть следующие факторы:
В аминах имеются связи С–Н и С–C (их характеристика уже дана в части II, раздел 2.2), а также связи
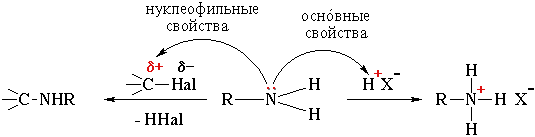
Исходя из распределения электронной плотности в молекуле и наличия неподеленной пары электронов на азоте, можно считать, что амины обладают основными и нуклеофильными свойствами:

Нуклеофильность - способность частицы предоставить электронную пару на образование связи с углеродом или с другим положительно заряженным атомом, кроме протона (H+). Стремление отдать пару электронов протону называется основностью.
Кроме того, атом азота в аминах имеет самую низкую для этого элемента степень окисления (-3). Поэтому амины могут вступать в реакции окисления по связям