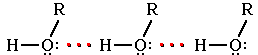
Ассоциация молекул ROH
2.4. Водородные связи и физические свойства
Следствием полярности связи О–Н и наличия неподеленных пар электронов на атоме кислорода является способность гидроксисоединений к образованию водородных связей (часть I, раздел 4.11).
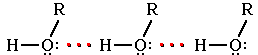
Это объясняет, почему даже низшие спирты – жидкости с относительно высокой температурой кипения (т.кип. метанола
Образование водородных связей с молекулами воды способствует растворимости гидроксисоединений в воде:
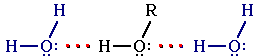
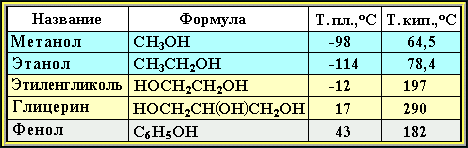
Способность растворяться в воде уменьшается с увеличением углеводородного радикала и от многоатомных гидроксисоединений к одноатомным. Метанол, этанол, пропанол, изопропанол, этиленгликоль и глицерин смешиваются с водой в любых соотношениях. Растворимость фенола в воде ограничена.
 Видеоопыт "Физические свойства одноатомных спиртов".
Видеоопыт "Физические свойства одноатомных спиртов".