7.3. Свойства аренов
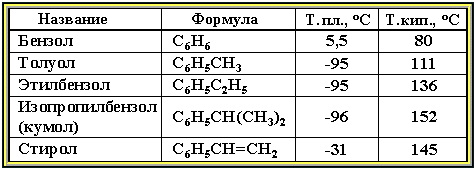
Физические свойства. Бензол и его ближайшие гомологи – бесцветные жидкие вещества (см. табл.), нерастворимые в воде, но хорошо растворяющиеся во многих органических жидкостях. Легче воды. Огнеопасны. Бензол токсичен (поражает почки, печень, костный мозг, кровь).

 Видеоопыт "Изучение физических свойств бензола".
Видеоопыт "Изучение физических свойств бензола".По химическим свойствам арены отличаются от предельных и непредельных
углеводородов. Это объясняется особенностями строения бензольного
кольца. Делокализация шести
Поэтому арены не склонны вступать в реакции присоединения или окисления,
которые ведут к нарушению ароматичности.
 Видеоопыт "Отношение бензола к бромной воде и раствору KMnO4".
Видеоопыт "Отношение бензола к бромной воде и раствору KMnO4".
Для аренов более характерны реакции, идущие с сохранением ароматической системы, а именно, реакции замещения атомов водорода, связанных с циклом.
Наличие областей повышенной π-электронной плотности с двух сторон
плоского ароматического цикла ведет к тому, что бензольное кольцо
является нуклеофилом и в связи с этим склонно подвергаться атаке
электрофильным реагентом. Таким образом, для ароматических соединений
наиболее типичны реакции электрофильного замещения.
Механизм электрофильного замещения обозначается символом SЕ
(по первым буквам английских терминов: S – substitution [замещение],
E – electrophil [электрофил]).
Другие реакции (присоединение, окисление), в которых участвуют делокализованные углерод-углеродные связи бензольного кольца и нарушается его ароматичность, идут с трудом.