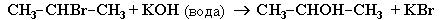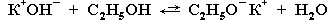
Почему для дегидрогалогенирования используется раствор щелочи в спирте, а не в воде?
В растворе КОН (или NaOH) в этиловом спирте С2Н5ОН присутствуют
ионы
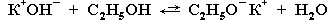
Ион С2Н5О- является более сильным основанием и легче, чем ион ОН-, отщепляет протон Н+ от галогеналкана. Это объясняется тем, что отрицательный заряд иона С2Н5О- более высок за счет смещения электронной плотности от этильной группы С2Н5 к атому кислорода (+I-эффект алкильной группы):
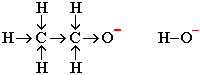
Отщепление атома водорода (в форме Н+) от галогеналкана сопровождается отрывом галогена (Hal-), и в результате образуется двойная связь:
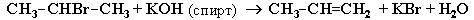
При использовании водного раствора КОН, содержащего ионы ОН- (это более слабое основание), преимущественно идет реакция не отщепления, а замещения: