4.3.1. sp3-Гибридизация (тетраэдрическая)
Одна s- и три р-орбитали смешиваются, и образуются четыре равноценные по форме и энергии sp3-гибридные орбитали.

Орбитальная модель атома в sp3-гибридизованном состоянии.
VRML-модель (109,8 Кб).
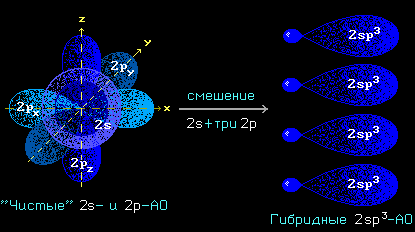
Схема sp3-гибридизации атомных орбиталей.
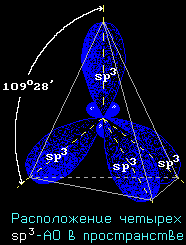 Оси sp3-гибридных орбиталей направлены к вершинам правильного тетраэдра. Тетраэдрический угол между ними равен 109°28', что соответствует наименьшей энергии отталкивания электронов.
Оси sp3-гибридных орбиталей направлены к вершинам правильного тетраэдра. Тетраэдрический угол между ними равен 109°28', что соответствует наименьшей энергии отталкивания электронов.
- Впервые идею о направленности единиц сродства (валентностей) атома углерода по углам тетраэдра независимо друг от друга выдвинули в 1874 г. Вант-Гофф и Ле Бель.
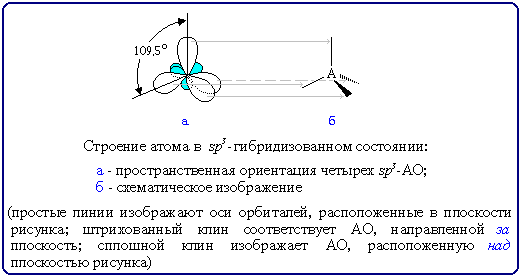
Переход от орбитальной модели (а) к пространственной формуле (б).
См. также рисунок. На примере молекулы метана показаны объемные модели и пространственная (стереохимическая) формула молекулы с
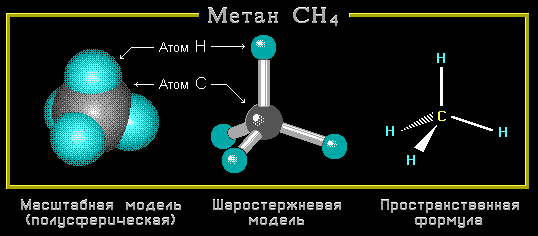

Модель молекулы метана
Cтроение молекулы этана C2H6 иллюстрируют рисунок и анимация.
- sp3-Гибридизованное состояние свойственно атому, если сумма числа связанных с ним атомов и числа его неподеленных электронных пар равна 4 (схема).
Это состояние характерно для атомов С, N, O и др., соединенных с другими атомами одинарными связями (sp3-атомы выделены красным цветом):
- Следствием тетраэдрического строения sp3-атома является возможность существования двух оптических стереоизомеров у соединения, содержащего такой атом с четырьмя разными заместителями (Вант-Гофф, Ле Бель, 1874).