3.2.2.3. Неполярная ковалентная
связь
Неполярная (симметричная)
ковалентная связь – связь между атомами с равной электроотрицательностью
(Δχ = 0) и, следовательно, равномерным распределением электронной плотности
между ядрами атомов:
H — H,
F — F, Cl — Cl, O = O, N ≡ N и т.п.
Неполярными являются также связи между одинаковыми атомными группировками.
Например, связь C—C в молекуле H3C—CH3.
Дипольный момент неполярных связей равен 0.
Связи между одинаковыми атомами, имеющими различное окружение, к неполярным не относятся.
Например: H3C—CH=O (ацетальдегид), H3C—COOH (уксусная кислота)
(дипольные моменты связей C—C 2,7 D и 1,7 D, соответственно).
Связь С — Н в предельных углеводородах (например, в СН4) считается практически
неполярной, т.к. Δχ = 2,5(С) – 2,1(Н) = 0,4 (дипольный момент связи 0,2 D).
Следует отметить, что в непредельных углеводородах (CH2=CH2, CH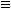 CH, RC
CH, RC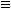 CH и т.п.) электроотрицательность углерода выше и связь С — Н
более полярна (особенно, если атом Н связан с углеродом, имеющим тройную
связь: H–C
CH и т.п.) электроотрицательность углерода выше и связь С — Н
более полярна (особенно, если атом Н связан с углеродом, имеющим тройную
связь: H–C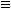 C–H, RC
C–H, RC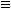 C–H).
C–H).
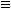 CH, RC
CH, RC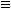 CH и т.п.) электроотрицательность углерода выше и связь
CH и т.п.) электроотрицательность углерода выше и связь 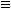 C–H, RC
C–H, RC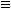 C–H).
C–H).
 CH, RC
CH, RC CH и т.п.) электроотрицательность углерода выше и связь
CH и т.п.) электроотрицательность углерода выше и связь  C–H, RC
C–H, RC C–H).
C–H).